Echinacea é uma erva perene da família composta echinacea, que está incluída na “United States Pharmacopoeia” como uma das fontes de base medicinal da echinacea. É naturalmente distribuído no centro-leste dos Estados Unidos e no sul do Canadá, e historicamente é uma medicina tradicional dos índios norte-americanos. Estudos farmacológicos mostraram que a equinácea tem efeitos imunológicos, anti-inflamatórios e antivirais. Tornou-se uma das ervas de reforço imunológico mais usadas no mundo e é usada como suplemento dietético. Os principais componentes eficazes da echinacea, incluindo derivados de ácido cafeico, alquil amida, polissacarídeo e óleo volátil e assim por diante, incluindo echinosídeo, um tipo de derivado de ácido cafeico, foram material representativo da erva echinacea, pode inibir células tumorais, antienvelhecimento, diabetes e outros benefícios, mas devido ao seu conteúdo ser baixo e difícil de separar, requisitos mais altos para o instrumento, a medição é relativamente difícil.
- Materiais de teste
As plantas de equinácea usadas neste experimento foram colhidas em agosto de 2020 no pico do período de floração da equinácea e armazenadas em quatro partes: caule, folha, raiz e cabeça, após serem secas à sombra a -20 ℃. O equipamento é cromatógrafo de fase líquida de alto efeito Agilent1100, detector externo roxo Agilent-G-1315B-DAD, máquina de desgaseificação em linha de espaço real Agilent322A, espectrômetro de cores HPChem-Station, britador universal de alta velocidade DFY-400 swing, análise eletrônica T2000Y, Instrumento de limpeza de ondas ultrassônicas SK82001HC, máquina centrífuga TG-16W.
Os reagentes incluem acetonitrila, metanol, ácido fosfórico, ácido acético glacial, etanol e outros reagentes puros cromatográficos, a água é água pura; Pó de Equinosídeo(De Rainbow Biotechnology Co., LTD., conteúdo ≥ 98% por HPLC).
2. Método de teste
Preparação da fase móvel
Colocação de solução de ácido fosfórico a 0.1%: remover com precisão 1.00ml de solução de ácido fosfórico em um balão volumétrico e usar água pura para manter o volume em 1000mL. Agite bem e ultrassônico por 5min para tornar a solução totalmente misturada. Em seguida, filtre-o com um dispositivo de filtro a vácuo e, em seguida, ultrassônico para remover bolhas. A configuração da solução de ácido acético glacial a 0.1%: remova com precisão 1.00 ml de solução de ácido acético glacial em uma garrafa volumétrica, use água pura para manter o volume constante em 1000 ml, agite bem, ultrassônico por 5 min para tornar a solução totalmente misturada e, em seguida, filtre com um dispositivo de filtro a vácuo e ultrassônico para remover bolhas.
Elaboração de padrões
O echinacoside padrão 0.01g foi pesado com precisão, dissolvido em álcool etílico a 70% e, em seguida, em frasco de volume constante de 10 mL, preparado em 1mg·mL-1 de licor mãe da substância de referência. Absorva com precisão 1mL da solução-mãe da substância de referência Echinosídeo, coloque-o em um frasco de volume de 10mL rotulado, dilua-o com álcool etílico a 70% até o grau de precisão, agite bem, prepare 0.1 mg·mL-1 de solução de armazenamento de substância de referência, deixe em repouso , em seguida, filtre com membrana microporosa (0.45 μm), o filtrado é a solução padrão de Echinosídeo.
Preparação de solução
Os diferentes materiais de equinácea foram secos e pulverizados separadamente e peneirados em 100 mesh. Pesar uma certa quantidade de cada amostra de pó medicinal, pesar com precisão, adicionar álcool etílico a 70%, volume constante de 10 mL, rotular, agitar bem, ultrassônico (40kHz) por 20min e mergulhar a frio em geladeira a 4 ℃ por 24h. A extração foi seguida por ultrassom (40kHz) por 20 min e centralização (3500r·min-1) por 10min. Absorver o sobrenadante e adicionar etanol 70% a 25 mL, agitar bem e colocar, filtrar com membrana microporosa (0.45μm), o filtrado é o líquido teste de cada amostra.
A análise dos dados
O software SPSS17.0 foi usado para análise de significância. P≤ 5% indicou diferença significativa. Software Excel2007 para confecção de curva padrão e cálculo de desvio padrão relativo (RSD); Para cada grupo de dados, foram realizados três grupos de testes paralelos para obter o valor médio.
3. Resultados e análise
Otimização da coluna cromatográfica
A fase móvel foi acetonitrila-ácido fosfórico a 0.1% (21∶79, v/v). O comprimento de onda de detecção foi de 330nm, a temperatura da coluna foi de 30 ℃, o volume de injeção foi de 10μL e a taxa de fluxo foi de 1.0 mL·min-1. Comparado com Agilent (tc-c185 μm 4.6 mm × 250 mm) e Diamonsil (5 μm C18, 4.6 mm × 250 mm), a separação da solução padrão de ecolina foi melhor pela análise da solução padrão. Os resultados mostraram que Agilent (TC-c185 μ m4.6 mm×250 mm) teve um melhor efeito de separação no pineosídeo.
Otimização da fase móvel e modo de eluição
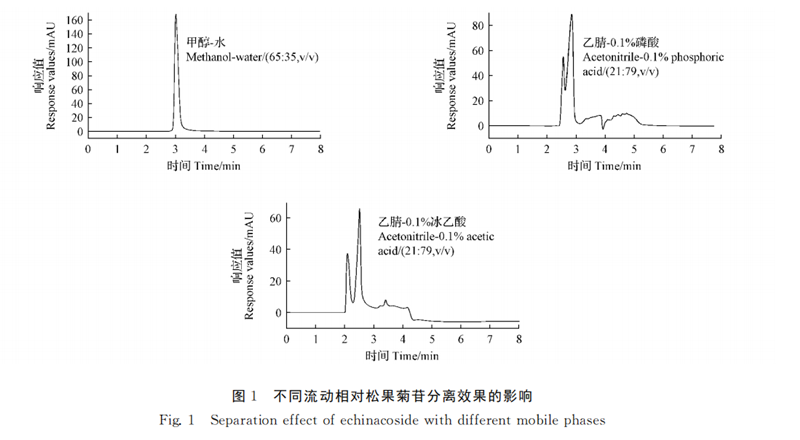
Agilent (TC-C185μm 4.6 × 250mm) foi selecionado, o comprimento de onda de detecção foi de 330nm, a temperatura da coluna foi de 30 ℃, o volume de injeção foi de 10μL e a taxa de fluxo foi de 1.0 mL·min-1. A separação da solução padrão de echinacoside com a fase móvel de metanol-água (65∶35, V/V), acetonitrila-0.1% de ácido fosfórico (21∶79, V/V) e acetonitrila-0.1% de ácido acético glacial ( 21∶79, V/V) foi investigado. Os resultados mostraram que a taxa de separação de echinacoside foi melhor quando metanol-água (65∶35, V/V) foi usado como fase móvel (FIG. 1).
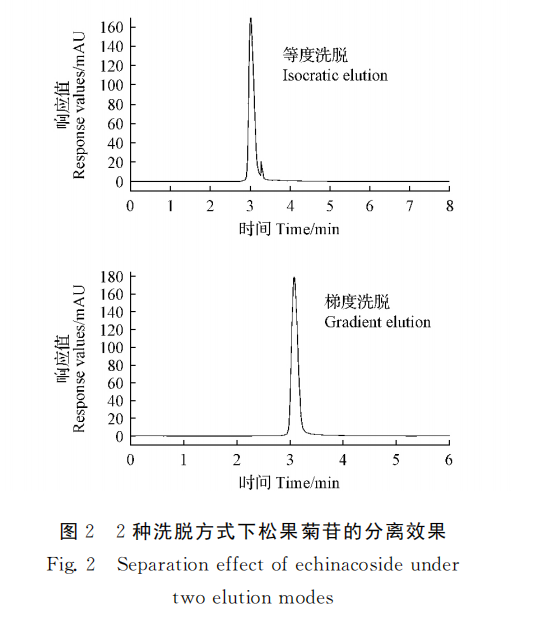
A separação do pinhiosídeo por lavagem de isograu de álcool metílico-água em fase móvel (65∶35, V/V) e lavagem de gradiente foram comparadas. Os resultados mostraram que a solução padrão de echinacoside foi bem separada sob eluição em gradiente, e o procedimento de eluição específico foi o seguinte: O gradiente de eluição da fase móvel água (A) e metanol (B) foi de 58% B (0 ~ 1 min, v/V), 58% ~ 62% B (1 ~ 2 min, V/V), 62% ~ 65% B (2 ~ 4 min, V/v), 65% ~ 58% B (4 ~ 8 min, V/ V). O grau de separação do pineosídeo foi o melhor (FIG. 2).
Otimização do comprimento de onda de detecção
A absorbância do echinacoside em 254, 327, 330 e 360 nm foi comparada. Finalmente, a absorbância do echinacoside foi maior quando o comprimento de onda foi de 330nm.
Otimização da temperatura da coluna: O efeito de separação do echinacoside na temperatura da coluna de 20, 25, 30, 35 ℃ foi comparado. Os resultados mostraram que o efeito de separação do pico cromatográfico do echinacoside foi bom quando a temperatura da coluna foi de 30 ℃.
As condições cromatográficas
As condições cromatográficas otimizadas foram as seguintes: coluna cromatográfica AGI-lent (TC-c185 μ m4.6 mm×250mm), fase móvel metanol-água, vazão 1.0 mL·min-1, comprimento de onda de detecção 330nm, temperatura da coluna 30 ℃, volume de injeção 10μL, eluição gradiente.
Teste de precisão
A solução padrão de echinacoside foi injetada 9 vezes consecutivas para calcular o RSD da área do pico. Os resultados mostraram que a área do pico RSD do echinacoside foi de 0.81%, indicando que a precisão do instrumento foi boa.
Teste de estabilidade
Prepare 0.1 g do mesmo pó de amostra de equinácea e a solução de amostra e injete 10μL em 0, 2, 4, 6, 8, 10, 12 e 24h, respectivamente. Analise a amostra por 8 vezes consecutivas de acordo com as condições cromatográficas mencionadas acima e calcule o valor RSD da área do pico. RSD de pinocyside foi de 0.50%, e o desvio padrão relativo foi de 5%. Os resultados mostraram que a solução testada ficou estável em 24h.
Teste de repetibilidade
Prepare 6 amostras do mesmo pó de amostra de equinácea, 0.1 g para cada amostra e a solução da amostra para injeção de amostra e análise nas condições cromatográficas mencionadas acima. O RSD da área do pico do echinacoside foi de 2.23%. Os resultados mostraram que o método teve boa repetibilidade.
Teste de recuperação
Os últimos 6 pós de echinacoside com concentrações conhecidas foram pesados com precisão e divididos em concentrações altas e baixas. Dados relevantes mostraram que, ao medir a taxa de recuperação, a fase de dosagem apropriada deve ser 0.5 ~ 2.5 vezes o conteúdo do grupo de teste. Adicionando 10μg·mL-1 de pinosídeo, o conteúdo da amostra foi 2 vezes o conteúdo da amostra. De acordo com a solução projetada e as condições cromatográficas do método padrão externo para calcular a concentração, calcule a recuperação de cada composto e a recuperação do valor RSD.
Taxa de recuperação marcada (%) = (valor medido da amostra de teste marcada – o valor medido da amostra)/escalar ×100.
A taxa de recuperação de echinacoside foi calculada pela fórmula acima. Ao medir a taxa de recuperação, o limite permitido da taxa de recuperação é de 80% ~ 120%, e o desvio padrão relativo está dentro de 5% quando o conteúdo do componente testado é menor ou igual a 1mg·L-1. Os resultados foram apresentados na Tabela 3, que mostrou que a recuperação do echinacoside variou de 88.03% a 97.88%, e a recuperação média foi superior a 93%. O RSD foi de 2.17% em baixa concentração, 0.38% em alta concentração e 1.28% em nível normal, o que atendeu aos requisitos de submissão de trabalhos. Mostrou que a taxa de recuperação foi boa e o método viável.
Determinação do conteúdo da amostra
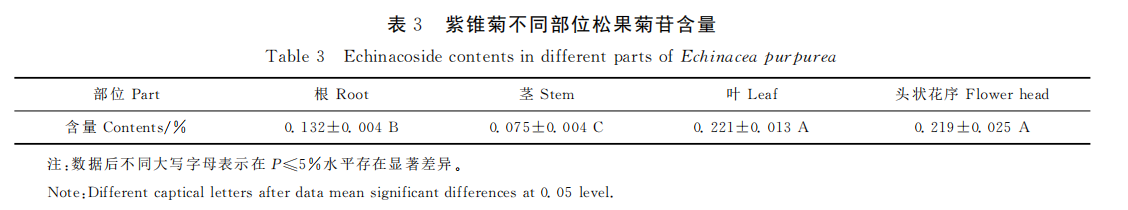
A raiz, caule, folha, inflorescência e casca de inflorescência de equinácea foram medidos com precisão com 0.1 g de pó, e a solução de teste foi preparada de acordo com o método descrito acima e as amostras foram analisadas sob as condições cromatográficas especificadas, e o conteúdo de echinacoside em cada parte foi calculada pelo método do padrão externo. Cada amostra foi medida três vezes em paralelo. Echinacea apresentou diferentes teores de echinacoside em diferentes partes. O teor de equinacosídeo nas folhas foi o mais alto (0.221%), o teor de equinácea na cabeça foi de 0.219%, não significativo, mas significativamente maior do que nas raízes (0.132%), e o teor de equinacosídeo nos caules foi o mais baixo (0.075%).
A separação e análise do echinacoside são difíceis e não existe um método unificado. Teste comparando a coluna cromatográfica diferente, a temperatura da coluna, o comprimento de onda de detecção, a fase móvel e o modo de análise quantitativa de glicosídeos de eluição de equinácea, a influência do método de análise quantitativa de equinácea otimizada, o método de análise de separação otimizado para melhorar a forma do pico cromatográfico, após a investigação da metodologia mostram que o método de análise quantitativa é estável, preciso e reprodutível. O método é simples e viável. O HPLC otimizado foi realizado em uma coluna Agilent (tc-c185 μ m4.6 mm × 250 mm) com um comprimento de onda de detecção de 330 nm, temperatura da coluna de 30 ℃, um volume de amostra de 10 μL, fase móvel foi metanol-água, taxa de fluxo de 1.0 mL.min-1, eluição em gradiente.
Os resultados mostraram que o conteúdo de echinacoside na família Echinacea e Echinacea angustifolia e Echinacea pallida têm um teor mais elevado do que o de Echinacea purpurea, e o teor de echinacoside na parte aérea foi superior ao da parte subterrânea. BINNS relatou que as raízes de equinácea produzidas no Canadá variaram em 0% ~ 0.054%, e as raízes de equinácea continham um alto teor de echinacoside, até cerca de 0.6%. Os resultados mostraram que o teor de echinacoside nas raízes da Echinacea branca de três anos foi de 0.596%. De acordo com esta pesquisa, o teor de echinacoside de Echinacea purpurea variou muito em diferentes partes variando de 0.075% a 0.221%, folhas e cabeças foi maior que nas raízes, e os caules basais foram os mais baixos. Os fabricantes de extrato de equinácea na China e na Índia atualmente têm concentrações de equinosídeos que variam de 0.01% a 0.23%, dependendo da origem.